La normativa vigente de ensayos clínicos establece que el promotor es el último responsable de la seguridad de los pacientes y de garantizar la fiabilidad de los resultados de estos ensayos. Cuando el promotor externaliza en una CRO el ensayo clínico, debe tener plena confianza en que la CRO va a cumplir con estas dos responsabilidades. Esto hace que la elección de la CRO sea un punto crítico en el proceso de evaluación del riesgo del ensayo clínico, por lo tanto, hay que introducir herramientas que lo controlen. Esta herramienta es el PNT: Auditoría de Calificación de CROs.
* Con la colaboración de Fernando García Alonso. Director General de Investigación y Desarrollo. Farmalider.
Los ensayos clínicos en Europa están regulados por el Reglamento (UE) Nº 536/2014 y por las GCP, ICH E6 (R2).
Los objetivos fundamentales de las GCP son:
• Garantizar la seguridad del paciente.
• Garantizar la fiabilidad de los datos y, en consecuencia, de los resultados del ensayo clínico.
Esta regulación establece que el promotor es el último responsable de que el ensayo clínico se ejecute de acuerdo con la normativa vigente, lo que le condiciona a tener un departamento de garantía/control de calidad que se responsabilice de vigilar y asegurar que los ensayos se realizan cumpliendo dicha normativa. Además, el departamento de garantía de calidad ha de ser totalmente independiente en la toma y ejecución de decisiones, sin estar condicionado por el departamento de clínica.
Hoy en día, casi todos los promotores externalizan en una Clinical Research Organitation (CRO) gran parte de las tareas y servicios que implican la ejecución de un ensayo clínico. Estas CROs también están obligadas a implementar un sistema de garantía/control de calidad que asegure que cumplen y trabajan de acuerdo con la normativa vigente. Aun así, aunque el promotor externalice parte, o todos los servicios de un ensayo clínico a una CRO, la última responsabilidad sobre la seguridad de los pacientes y la fiabilidad de los datos, y en general sobre el cumplimiento de toda la normativa, recae siempre sobre el promotor.
En el momento en que el promotor transfiere servicios a una CRO, los departamentos de clínica y de garantía de calidad de ambos deben trabajar en conjunto. Por lo que, llegados a este punto, es esencial para el éxito del ensayo clínico, que la CRO y el promotor estén alineados en su manera de trabajar, es decir, ambos han de tener los mismos principios y valores, la misma disciplina en el trabajo, los mismos estándares de calidad y trato con el equipo humano.
El promotor tiene que estar seguro de que está trabajando con la CRO más apropiada a sus necesidades por varias razones:
• El elevadísimo coste de los ensayos clínicos, ya que hablamos, en la mayoría de los casos de millones de euros.
• El promotor y la CRO van a trabajar juntos e intensamente durante un largo periodo de tiempo, por lo que cuanto más parecidos sean sus valores y su modo de trabajo, mejor será la cooperación entre ellos y más confianza se generará.
• Expectativas de negocio del promotor y retorno de la inversión.
• Desde un punto de vista regulatorio, el promotor tiene que estar muy seguro de que la CRO cumple con la normativa vigente, porque si en la CRO hay un problema de infracción de la legislación (aunque la CRO también está obligada por ley a cumplir con la normativa, y por eso tiene su propio departamento de garantía y control de calidad), es el promotor el que, al final, tendrá una dificultad con las autoridades competentes y con su producto.
Pero ¿cómo elige el promotor la CRO? Esta es una de las decisiones cruciales para los promotores ya que es mucho lo que hay en juego, por lo que esta elección debe ser incluida como uno de los elementos críticos en el análisis del riesgo del estudio, lo que implica que hay que introducir procedimientos o herramientas que logren disminuir y controlar el peligro de este punto crítico, hasta un nivel que para el promotor sea aceptable. Desde mi experiencia, la mejor herramienta que nos va a ayudar a reducir y controlar este punto crítico, es decir, la elección de la CRO, son las Auditorías de Calificación para CROs.
Esencialmente, a través de las Auditorias de Calificación, el promotor trata de determinar si el nivel de cumplimiento de las áreas fundamentales de la CRO satisface sus requerimientos.
Las Auditorías de Calificación de CROs deben formar parte de los Procedimientos Normalizados de Trabajo (PNT) del departamento de garantía y control de calidad de los promotores. Y aunque es la persona de garantía de calidad quien debe estar presente y realizar todo el proceso de selección de la CRO usando la PNT ya mencionada, es muy acertado si otra persona del departamento de clínica también está presente durante ese proceso, ya que son los departamentos de clínica del promotor y de la CRO quienes de manera más complementaria y sinérgica van a trabajar durante largos periodos de tiempo.
El enfoque de las Auditorías de Calificación de CROs es muy diferente al de las auditorías de ensayos clínicos. Mientras que en estas últimas tenemos y analizamos datos reales del ensayo, en las primeras el ensayo aún no ha comenzado y se van a analizar otras áreas fundamentales de las que hablaremos más abajo. El enfoque de las Auditorías de Calificación ha de ser estratégico, por lo que hay que intentar anticiparse a las posibles deficiencias que pueda tener la CRO al ejecutar el estudio, y para esto, para identificar estas deficiencias, hay que proyectar cómo se van a acoplar las características y puntos críticos del estudio y de la empresa, en la filosofía y en las características de la CRO. A partir de estas deficiencias identificadas, y de otros elementos que son siempre críticos en un ensayo, creamos las áreas fundamentales que hay que analizar en la CRO, y que nos van a ayudar a conocer la verdad o la realidad de cómo trabaja la CRO y de cómo será la cooperación promotor-CRO. Estas áreas y su contenido van a cambiar en función del promotor y del ensayo clínico; y en mi experiencia se puede resumir en tres:
Due diligence: Es un cuestionario para analizar y evaluar las áreas operativas de la CRO. A continuación, propongo algunas de éstas y doy ejemplos.
• Personal y Formación: tipo de formación en GCP, formación continua, renovación del personal, asignación a estudios, cómo se forma a las personas en los estudios (un periodo de comonitorización con un monitor senior es lo más efectivo).
• Externalización de servicios: Actividades que externalizan (como el eCRF o la monitorización en países donde no existe sede), cómo aseguran la calidad de los proveedores.
• Garantía y control de calidad: listado de PNT, frecuencia de auditorías internas, si han sido auditados por clientes o inspeccionados por autoridades regulatorias (hallazgos críticos de estas inspecciones), validación de sistemas informáticos, procedimiento de escalado y resolución de desviaciones con CAPA plan.
• Experiencia previa en ensayos clínicos: áreas terapéuticas, fases del ensayo, número de pacientes, nacionales o internacionales, número de centros.
• Sistemas informáticos usados en el estudio: certificados para el uso de programas estadísticos.
• Project Manager: herramientas del Project Manager y Clinical Research Associate de la CRO para gestionar el ensayo (aquí es importante que la CRO haga una demostración del sistema de gestión del estudio), plan de comunicación.
• Monitorización: monitorización basada en el riesgo.
• Muestras biológicas: PNT de gestión de diferentes tipos de muestras biológicas.
• Data management: cómo aseguran la integridad de datos, eCRF.
• Medical writing: ¿existe un médico?
• Localización de la CRO: Depende del tipo de ensayo clínico. Si es internacional, es recomendable que la CRO tenga delegaciones en todos los países en los que tendremos centros ya que, si no es así, externalizarán los servicios de submission y monitorización, lo cual significa que en el estudio intervienen proveedores de servicios que el promotor no ha auditado. Si el estudio es nacional, es mejor que la CRO tenga delegación en el mismo país.
Presupuesto: Cualquier valor extremo a la baja o a la alta llama la atención negativamente.
Interés que muestra la CRO: Dos factores son importantes para valorar este interés, y son el tiempo de respuesta y la adaptación a nuestras necesidades. Sobre todo, en las fases tempranas de selección de la CRO, cuando aún es sabido que existen varias CRO compitiendo, es clave que las CRO que están siendo evaluadas, respondan relativamente pronto a tus cuestiones y que, por otro lado, quieran y puedan adaptarse a tus necesidades. En definitiva, estos dos factores nos indican el interés que tiene la CRO en ser elegida y en trabajar con nosotros.
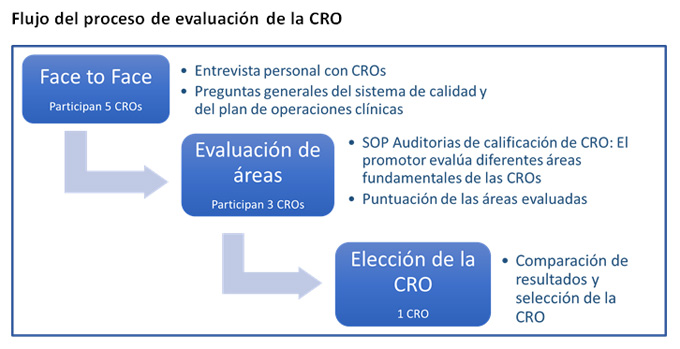
Las Auditorías de Calificación son una parte de todo el proceso de selección de la CRO, el primer paso es conocer cara a cara a un máximo de 5 CROS, y de la información que saquemos de este primer encuentro, podremos decidir a qué CROs vamos a hacer una Auditoría de Calificación. Si en este primer encuentro se confirma que una o varias de ellas, no tiene experiencia en el área terapéutica, no merece la pena seguir adelante e implicar a la CRO ni a nosotros mismos como promotores, en todo el trabajo que supone la Auditoría de Calificación. Lo importante de este primer encuentro es que las personas con las que estamos entrevistándonos nos den confianza en su manera de trabajar. No importa si los miembros de la CRO tienen una gran presentación de power point, importa lo que nos dicen, y cómo lo dicen. Tampoco importa si no pueden responder a algunas de nuestras preguntas en el momento de la entrevista, ya que muchas veces pertenecen al departamento de desarrollo de negocio, pero sí importa que, si no pueden responder en ese momento, sean ágiles en buscar en su equipo una respuesta, y nos la envíen en un plazo corto. En este primer encuentro pueden participar hasta cinco CROs, y seleccionaremos un máximo de tres para hacer la Auditoría de Calificación. Una vez que se tienen los resultados de la evaluación de la auditoría de las tres CROs, está en las manos del promotor elegir la CRO finalista.
Cuando la selección de la CRO ya se ha llevado a cabo, los departamentos de garantía/control de calidad y clínica deben seguir revisando si los valores de las áreas evaluadas, u otras nuevas que aparezcan, se mantienen donde establecimos.
En general, el proceso de ejecución del ensayo clínico es muy dinámico, van a surgir variables con las que no contábamos, y debemos gestionarlas de manera que se cumplan los dos principios de la normativa regulatoria: protección de la seguridad de los pacientes y fiabilidad de los datos. Por eso, cuanto mejor conozcamos a priori la manera de trabajar de la CRO, más confianza tendremos en que cuando surjan estas complicaciones, van a ser gestionadas por la CRO elegida de la manera que nosotros, como promotores y últimos responsables legales, sabemos que debe ser para satisfacer la normativa de ensayos clínicos y nuestros valores de empresa.
Fuentes Consultadas:
The Nuts & Bolts of CRO Selection, by Joelle Herman, President &Principal Sr. Consultant of Neo Trials, LLC.
GCP Qualification Audits: Choosing Quality Contractors and Sites.
Risk Management in Clinical Trials: The New ICH E6 Focus, by Dr. Susan Leister.














