En numerosas ocasiones la investigación clínica se limita a añadir una nueva herramienta al arsenal médico disponible. Sin embargo, en otras muchas ocasiones la investigación clínica aporta algo más, es capaz de modificar los procedimientos y percepciones de los médicos. Promueve el inconformismo de la comunidad médica, que desde ese momento exige unos nuevos estándares de eficacia para sus tratamientos. Vemos como ejemplo el caso particular de Secukinumab, inhibidor de la interleuquina 17A.
Por todos es sabido que la investigación es uno de los motores de esta sociedad, o así debería serlo. Más aún en el ámbito biosanitario, dónde ésta investigación se traduce en una mejora de la salud y calidad de vida de los ciudadanos.
Es precisamente ahí donde más se puede apreciar cómo la investigación clínica, a través de los ensayos clínicos, es una etapa esencial para que se lleve a cabo la traslación desde el logro científico hasta la práctica clínica real.
Son numerosos los ejemplos de nuevas terapias, nuevos procedimientos o dispositivos médicos que llegan al mercado tras su investigación clínica año tras año. Aunque, si bien representan un avance, no afectan inmediatamente a la práctica clínica real. El médico toma sus decisiones en base a sus conocimientos, razonamientos e intuiciones, y los nuevos avances que día tras día se ponen a su disposición enfrentan alguna resistencia. Es por esto que muchos de estos avances no son incorporados a la práctica médica. Perdiéndose gran parte de “la magia” que todos los que trabajamos en este ámbito buscamos, cambiar la vida de los pacientes.
En ocasiones estos avances no se incorporan a la práctica médica no porque la investigación carezca de valor o no esté dirigida a cubrir una necesidad real, sino por el simple retraso existente entre estas dos fases. Tomemos como ejemplo los 15 años de retraso desde que los betabloqueantes mostraron su efecto sobre los pacientes con infarto de miocardio hasta que al menos el 62% de estos pacientes lo incorporaron como tratamiento de elección.1

Sin embargo, en otros muchos casos conseguimos ese efecto del que hablamos. La innovación y los resultados conseguidos en la investigación clínica se traduce en un avance sustancial, tangible, que afecta de forma directa a la práctica clínica real y modifica los procedimientos y decisiones de los médicos. Son estos casos los que podemos definir como éxitos rotundos.
Pongamos un ejemplo de cómo la investigación clínica cambia la percepción e incluso las necesidades del médico y pacientes. Es el caso del tratamiento de la psoriasis tras los buenos resultados obtenidos por la molécula inhibidora de la interleuquina 17A (IL-17A).
Esta molécula, Secukinumab, desarrollada por Novartis, no sólo tuvo unos muy buenos resultados clínicos, sino que consiguió cambiar la percepción de los médicos en cuanto a la respuesta que los fármacos para el tratamiento de esta enfermedad tenían. Desde la aparición de esta mólecula los estándares de medida de eficacia de referencia han pasado del Índice de Área de Gravedad de la Psoriasis 75 (PASI 75) a PASI 90 o PASI 100.
Este índice consiste en una medición de la severidad de la psoriasis en cuanto a descamación, induración y eritema en varias partes del cuerpo, así como el área del cuerpo afectada. Cuando nos referimos a un PASI 75 o PASI 90 hablamos de una mejoría del 75% o 90% de la psoriasis.
En los últimos años los profesionales que tratan esta enfermedad, dermatólogos en su mayor parte, ya no se conforman con resultados de PASI 75, sino que exigen un PASI 90 como “gold standard” en la medida de eficacia de estos fármacos. Pero este nuevo inconformismo no viene dado tan sólo por parte de los médicos, sino que también las agencias de medicamentos, FDA y EMA en este caso, exigen que los nuevos fármacos aporten algo más con respecto a los ya existentes y que, en el caso de la psoriasis, se exijan datos de PASI 90 para la aprobación de las nuevas moléculas.
Basta con observar el número de ensayos clínicos que utilizan esta medida, PASI 75 o PASI 90, para evaluar la eficacia de un fármaco contra la psoriasis para darnos cuenta de cómo ha cambiado el escenario en este ámbito (Figura 1). A partir de 2009 se observa un repunto drástico en el número de fármacos aprobados cuyos ensayos utilizan PASI 90, PGA 0/1 y IGA 0/1 (parámetros que reflejan un aclaramiento o casi aclaramiento de la piel) como medida de eficacia, mientras que fármacos aprobados cuyos ensayos utilizan PASI 75 van paulatinamente siendo cada vez menos, llegando a 2019 en el que el porcentaje moléculas aprobadas con ensayos clínicos con PASI 75 como medida de eficacia es 0. Esta tendencia refleja una mejoría en el manejo de la enfermedad y una elevación del objetivo terapéutico. Téngase en cuenta, además, que la investigación clínica se orienta a dar respuesta una necesidad no cubierta en la práctica médica, por lo que este cambio en la medida de eficacia usada en los ensayos clínicos es también un reflejo de las nuevas necesidades de los médicos.
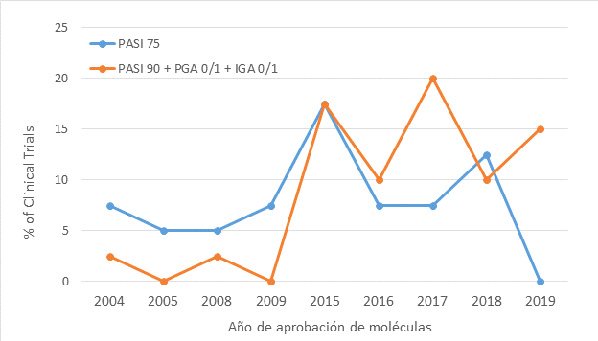
Figura 1. Años de aprobación de fármacos para la psoriasis y porcentaje de ensayos clínicos que utilizan PASI 75 o PASI 90, PGA0/1 y IGA0/1 como medida de eficacia. Numero de ensayos analizados, 40.2
En el caso particular de la psoriasis, el aumento constante de la eficacia de los nuevos fármacos representa una enorme mejoría en la calidad de vida de los pacientes ya que tiene un impacto positivo no solo a nivel dérmico, sino también psicológico.
Debemos tener en cuenta también que a menudo los pacientes de psoriasis padecen de estigma social y baja autoestima debido a la naturaleza estética de la enfermedad.
Usando el caso de una nueva molécula como Secukinumab en el ámbito de la psoriasis, podemos ver cómo la investigación clínica tiene un impacto real en la práctica médica. No sólo respecto a la mejoría clínica y la calidad de vida del paciente que una nueva molécula puede aportar. Sino que la investigación clínica realmente efectiva es aquella que consigue modificar la percepción del médico, aquella que le hace cambiar su práctica clínica y le hace no conformarse con los estándares que hasta ese momento eran los estipulados. En última instancia, el avance científico y el inconformismo que se respira en la investigación clínica, motor en la mayoría de los casos del avance científico, deben ser, y son, bien recibidos por la comunidad científico/médica ya que aportan un beneficio incalculable a la sociedad y a nuestra calidad de vida, haciendo, además, que la práctica médica avance y sea cada vez más efectiva y exigente.
1 Lenfant C. Clinical research to clinical practice. Lost in traslation? N Engl J Med. 2003;349:868-74.
2 Arch Dermatol. 2011 Apr;147(4):429-36. doi: 10.1001/archdermatol.2010.384. Epub 2010 Dec 20
Blauvelt A, et al. J Am Acad Dermatol 2017;76:405
BMJ. 2010 Feb 2;340:c147. doi: 10.1136/bmj.c147
Br J Dermatol. 2005 Jun;152(6):1304-12
Br J Dermatol. 2008 Mar;158(3):558-66. Epub 2007 Nov 28
Br J Dermatol. 2008 Nov;159(5):1177-85. doi: 10.1111/j.1365-2133.2008.08771.x
Br J Dermatol. 2015 Feb;172(2):484-93. doi: 10.1111/bjd.13348. Epub 2014 Dec 11
Br J Dermatol. 2016 Aug;175(2):273-86. doi: 10.1111/bjd.14493. Epub 2016 Jun 23
Br J Dermatol. 2019 Jun 19. doi: 10.1111/bjd.18232.
Dermatol Ther (Heidelb). 2018 Dec;8(4):571-579. doi: 10.1007/s13555-018-0265-y. Epub 2018 Oct 17.
Gordon KB, et al. N Engl J Med 2016;375:345
Griffiths CE, et al. Lancet 2015;386:541
https://clinicaltrials.gov/ct2/show/NCT01232283
https://clinicaltrials.gov/ct2/show/NCT02672852
J Am Acad Dermatol. 2007 Jan;56(1):31.e1-15. Epub 2006 Sep 6
J Am Acad Dermatol. 2008 Jan;58(1):106-15. Epub 2007 Oct 23.
J Am Acad Dermatol. 2015 Jul;73(1):27-36.e1. doi: 10.1016/j.jaad.2015.04.011. Epub 2015 May 14
J Am Acad Dermatol. 2015 Jul;73(1):37-49. doi: 10.1016/j.jaad.2015.03.049
J Am Acad Dermatol. 2017 Jan;76(1):60-69.e9. doi: 10.1016/j.jaad.2016.08.008. Epub 2016 Sep 20
J Am Acad Dermatol. 2018 Aug;79(2):266-276.e5. doi: 10.1016/j.jaad.2018.04.013. Epub 2018 Apr 14.
J Am Acad Dermatol. 2018 Aug;79(2):302-314.e6. doi: 10.1016/j.jaad.2018.04.012. Epub 2018 Apr 13
J Eur Acad Dermatol Venereol. 2015 Jun;29(6):1082-90. doi: 10.1111/jdv.12751. Epub 2014 Sep 22
Lancet. 2005 Oct 15-21;366(9494):1367-74
Lancet. 2008 May 17;371(9625):1665-74. doi: 10.1016/S0140-6736(08)60725-4
Lancet. 2008 May 17;371(9625):1675-84. doi: 10.1016/S0140-6736(08)60726-6
Lancet. 2018 Aug 25;392(10148):650-661. doi: 10.1016/S0140-6736(18)31713-6. Epub 2018 Aug 7
Lancet. 2019 Aug 17;394(10198):576-586. doi: 10.1016/S0140-6736(19)30952-3. Epub 2019 Jul 4
Lancet. 2019 Sep 7;394(10201):831-839. doi: 10.1016/S0140-6736(19)31773-8. Epub 2019 Aug 8.
Langley RG, et al. Br J Dermatol 2018;178:114
N Engl J Med. 2003 Nov 20;349(21):2014-22
N Engl J Med. 2010 Jan 14;362(2):118-28. doi: 10.1056/NEJMoa0810652
N Engl J Med. 2014 Jul 24;371(4):326-38. doi: 10.1056/NEJMoa1314258. Epub 2014 Jul 9
N Engl J Med. 2015 Oct;373(14):1318-28. doi: 10.1056/NEJMoa1503824
Reich K, et al. Br J Dermatol 2017;177:1014
Reich K, et al. J Am Acad Dermatol 2017;76:418















