|
 Albert Esteve
Albert Esteve
|
PMFARMA le ha entrevistado con motivo de este importante nombramiento y nos ha comentado la más reciente actualidad de la situación de este mercado en España y en Europa.
¿Cómo está evolucionando en Europa el mercado de la automedicación?
Habría que comentar dos aspectos; qué es el mercado de la automedicación y otra cosa distinta, cómo evoluciona. Desde el punto de vista de la evolución me gustaría destacar que el mercado Europeo en general y el español en particular evolucionan lentamente. En concreto, en España, el mercado de las EFP representa alrededor del 5% del mercado total, mientras en Europa se sitúa entre el 15 y 20%. En este sentido, el sector de las EFP en España tendrá que realizar un sobreesfuerzo si quiere llegar a conseguir las cuotas de participación europeas.
¿Cuáles son los factores que hacen que las EFP en España tengan tan poca vitalidad?
Los motivos son diversos. Los más destacables serían: un sistema de control de la publicidad demasiado rígido y limitativo; pocos productos de prescripción susceptibles de cambio a EFP por problemas regulatorios; el co-pago del paciente de la Seguridad Social es muy reducido y que en nuestro país existe un alto grado de financiación pública de los medicamentos. No olvidemos también los aspectos culturales del uso del medicamento en España. Todo ello conforma un entorno que no favorece el crecimiento de la automedicación en España.
Con todo, me gustaría señalar que en los últimos cinco años, el mercado español ha evolucionado positivamente en cuanto a disponibilidad de principios activos, indicaciones y hasta en la publicidad más creativa que se puede realizar ya con las EFP. El camino que nos falta por recorrer, es conseguir en España la flexibilidad que tienen países como Gran Bretaña o Alemania, por poner sólo dos ejemplos.
Como Presidente de la AESGP, ¿qué líneas básicas de actuación piensa impulsar en la política europea de la Asociación?
La AESGP agrupa las asociaciones nacionales de automedicación de los distintos países europeos y también a compañías farmacéuticas, multinacionales o no, presentes en este mercado.
Su principal objetivo es procurar y defender un entorno donde se pueda desarrollar la automedicación responsable de la mejor manera posible.
Un aspecto importante, y que nos preocupa a todos, es la sostenibilidad del sistema. La automedicación es un elemento clave que puede permitir que el estado del bienestar europeo actual pueda ser sostenible, es decir, que muchas de las consultas médicas que se producen en la actualidad y que, obviamente, representan una parte importante de los recursos sanitarios, se puedan tratar, en primera instancia, en la oficina de farmacia y, por supuesto, con tratamientos OTC. Este aspecto, que a primera vista puede parecer una obviedad, tiene una importancia económica extraordinaria.
Por otra parte, en estos momentos estamos muy implicados también con la propuesta de la nueva reforma de la legislación europea en torno a los denominados "productos de venta libre", que entrará en vigor en un año, o año y medio, a lo sumo.
Del borrador estudiado por la AESGP hay diversos aspectos que nos gustaría mejorar, y así se lo hemos hecho saber al Parlamento Europeo, uno de ellos es la creación de un entorno competitivo en relación con la automedicación responsable. Otro de los objetivos de la AESGP es conseguir que la presentación estudios/dossier para la obtención de switching o la ampliación de indicaciones sobre una molécula ya conocida, que haya necesitado investigación clínica adicional, pueda disfrutar de un período de protección de datos, cosa que reforzaría la innovación dentro de la industria OTC.
¿A qué se refiere con lo de protección de datos?
Salvando las distancias, sería como si de una patente se tratara. La innovación en OTC's es muy difícil y compleja. Por ejemplo, una compañía quiere conseguir una nueva indicación para su producto OTC, esta nueva indicación conlleva una investigación y desarrollo adicional; al tratarse normalmente de un principio activo con su patente de producto ya caducada y por tanto sin protección legal, ni exclusividad en el mercado, lo que la AESGP persigue es que las compañías que realicen éste desarrollo adicional para una ampliación de indicaciones, tengan el derecho de protección de los datos presentados como compensación a su esfuerzo en I+D. Este aspecto ya se da en los Estados Unidos, donde existe una protección de datos de tres años para las compañías que innovan en el mercado OTC con productos conocidos y que tuvieron su origen en la prescripción. En otras palabras, en Europa tenemos que proteger la innovación y creemos que las autoridades europeas son bastante favorables a esta aspiración de la industria.
No hay que confundir esto con la protección de patentes frente a los genéricos. No tiene nada que ver. Lo comento porque he detectado cierta confusión al respecto. Esta norma por la que estamos luchando, afectaría exclusivamente a los productos de automedicación.
¿Cómo se está abordando la regulación de los nutracéuticos en Europa?
En la actualidad, hay países en los que un producto determinado puede acogerse a este tipo de registro y otros en los que no se le permite, por lo que es preciso armonizar la legislación de este tipo de alimentos. Este es un tema complejo ya que muchas veces la frontera entre un nutracéutico y un producto OTC es difícil de distinguir, si le añadimos que la industria alimentaria en general está tendiendo cada vez más a la inclusión del concepto de salud en sus productos, el tema adquiere una mayor dimensión.
¿Las compañías que se dedican a fitoterapia e hierbas medicinales esgrimen que se les está complicando la existencia, desde varios frentes, incluida la propia industria farmacéutica tradicional, y que las futuras regulaciones pretenden dejarlos fuera de juego. ¿Qué opina usted al respecto?
AE. Por parte de la industria farmacéutica no hay ninguna voluntad en la dirección que usted apunta. Todo lo contrario. El mercado de la fitoterapia es tan válido como cualquier mercado farmacéutico. Lo que sucede es que algunas plantas de uso tradicional realizan "claims" o propuestas de salud mucho más fuertes que las que se le permite a una EFP, y esto es lo que no se debería producir. Todos podemos ver en establecimientos, que no son oficinas de farmacia, productos que realizan propuestas de indicaciones totalmente inaceptables. Este mercado debería ser regulado, al igual que sucede con las EFP. Hay que distinguir entre indicaciones terapéuticas y alegaciones de salud.
¿Para qué fecha se espera una regulación definitiva, o por lo menos, mucho más amplia del mercado de la automedicación?
Será a través de la directiva de la Unión Europea, que se espera que entre en vigor en el año 2004, y desde luego, será de mucho más alcance que la legislación actual.
¿Qué características diferenciales tiene el mercado americano de la automedicación, con relación al europeo?
Por ejemplo, la protección de datos que comentábamos antes, en los Estados Unidos es plenamente efectiva. La publicidad OTC también es diferente, aunque hay que señalar, que también la publicidad del mercado de prescripción es muy diferente, ya que ellos sí pueden realizar publicidad directa al paciente, a través de los grandes medios de comunicación.
La distribución también es diferente, ya que existen cadenas farmacéuticas, los drugstores, etc.
Grupos terapéuticos del mercado EFP en España (2001)
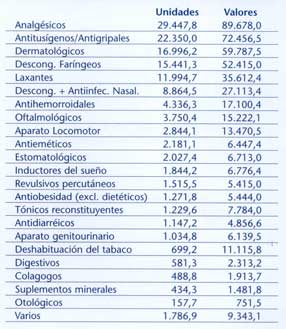
Valores en miles de euros.
Unidades en miles.
Fuente: ANEFP/IMS |
Con todo, y pese a las diferencias, el mercado de los Estados Unidos es un mercado de referencia, o mejor dicho, de comparación, sobretodo por el grado de flexibilidad que tiene en el mercado de la automedicación.
Esteve apostó por el mercado de la automedicación hace ya más de 15 años. Transcurrido este tiempo, ¿qué valoración hace de la evolución conseguida por la empresa?
La actividad de nuestro Grupo en el mercado de la automedicación se basa en dos segmentos: el mercado de OTC puro y el mercado de la parafarmacia con productos de alimentación infantil. Nuestra fuerza de ventas ha ido creciendo hasta llegar a la actualidad a un equipo de 25 personas. Uno de nuestros principales objetivos es ofrecer servicio al farmacéutico, aunque estamos orientados al consumidor, deseamos aportar a nuestro cliente un servicio excelente y una gama de productos innovadores. Nuestro principal interés se basa más en el ámbito estratégico que en el operativo.
|














