La generación de “evidencia”, “pruebas” en su traducción más correcta, en el mundo real (Real World Evidence, RWE) se ha convertido en una herramienta poderosa en la industria farmacéutica para ayudar a los laboratorios a demostrar el valor de sus tratamientos a reguladores, pagadores, proveedores, profesionales sanitarios y pacientes. Pero vayamos un paso atrás, ¿sabemos realmente qué es RWE?

RWE es el resultado del análisis de datos que se generan por la práctica clínica en el mundo real (Real Wold Data, RWD), incluyendo el uso de los medicamentos y demás intervenciones sanitarias. RWD y RWE se refieren, pues, a cualquier dato relevante que no se haya recopilado a través de un ensayo clínico aleatorizado (ECA).
Los ensayos clínicos están diseñados para probar si un medicamento o tratamiento funciona en condiciones controladas y específicas y, como tal, tienen una gran cantidad de criterios de inclusión y exclusión. Esto limita el número de pacientes elegibles para el ensayo clínico y también limita la posibilidad de generalizar los resultados del ensayo a otros pacientes con la enfermedad de interés. RWE agrega información a los resultados de los ensayos clínicos aleatorizados (ECA) al ofrecer datos de efectividad, no eficacia, y datos adicionales de seguridad en pacientes “reales” que muchas veces están polimedicados, es decir, aportan la experiencia que se obtiene sobre el nuevo tratamiento en el mundo real. Estas observaciones se pueden recopilar de una variedad de fuentes no intervencionistas, incluidos datos de visitas de rutina al hospital o al médico, registros de pacientes, dispositivos conectados, datos de prescripción, estudios observacionales y otros datos primarios y secundarios a nivel de paciente.
Dado que los estudios de RWE tienen pocos criterios de exclusión, representan una población de usuarios más realista. Las diferentes edades, comorbilidades, uso de medicamentos adicionales, nivel de cumplimentación de los tratamientos y comportamientos de atención médica de estas poblaciones, brindan nuevos conocimientos sobre la seguridad y efectividad de un tratamiento, y hacen posible identificar tendencias en subpoblaciones específicas. Los estudios del mundo real (RWE) también se pueden realizar durante un período de tiempo mucho más largo, a menudo con unos costes asociados muy inferiores a los estudios clínicos.
El uso de datos y “pruebas” del mundo real ayuda por lo tanto a cerrar la brecha de información del ECA para comprender la verdadera efectividad y el perfil de seguridad del producto una vez se usa fuera del ámbito del ensayo clínico.
Inteligencia Artificial (IA) como un catalizador de la generación de Real World Data (RWD) y de Real World Evidence (RWE)
Uno de los potenciales frenos del desarrollo de RWE es la elevada cantidad de datos sin procesar y la creciente complejidad de los conjuntos de datos. En este contexto, la Inteligencia Artificial y Machine Learning (IA/ML) se ha convertido en un conjunto de herramientas extremadamente útiles para poder generar bases de datos fiables (RWD) que posteriormente se pueden traducir en “pruebas” (RWE).
El siguiente esquema refleja cómo las herramientas de IA/ML pueden ayudar en todo el proceso de generación y procesamiento de datos y explotación de la evidencia para optimizar la práctica clínica habitual:
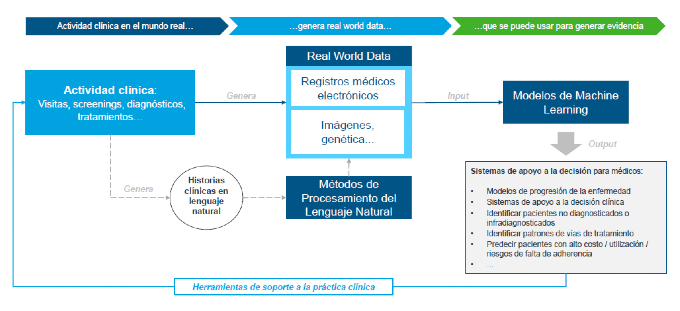
- Generación de datos: en muchas ocasiones la información de la actividad clínica está desestructurada y en lenguaje natural, como es el caso del texto incluido en las historias clínicas de los hospitales. Los algoritmos de procesamiento del lenguaje natural nos permiten procesar toda esta información y estructurarla de tal manera que se pueda obtener valor de una información que hasta ahora solo podía ser explotada de una manera muy poco eficiente.
- Explotación de evidencia: las herramientas de análisis tradicionales nos permiten hacer un análisis descriptivo de la información: ¿Qué ha pasado?. Sin embargo, las herramientas de IA/ML nos permiten obtener analíticas más avanzadas en las que podemos generar análisis predictivos (¿qué es probable que pase?) y prescriptivos (¿qué debería hacer?). Esto nos abre la puerta, por ejemplo, a la generación de herramientas de apoyo a la decisión para los clínicos:
o Modelos de progresión de la enfermedad
o Sistemas de apoyo a la decisión clínica
o Identificar pacientes no diagnosticados o infradiagnosticados
o Identificar patrones de vías de tratamiento
o Predecir pacientes con alto costo / utilización / riesgos de falta de adherencia
o ...
Casos reales de uso de la IA/ML como motor de generación de evidencia
Como se ha descrito en las anteriores secciones las herramientas de IA/ML suponen un motor para el desarrollo de “pruebas” adicionales sobre el valor de las nuevas intervenciones sanitarias, entre ellas los medicamentos, que ayuden al correcto posicionamiento de las distintas opciones terapéuticas y a la mejora de la calidad asistencial. En este sentido, los últimos avances en la materia nos indican que se está trabajando en 4 grandes áreas de modelos de IA/ML en RWE:
- Herramientas de detección de la enfermedad
- Herramientas de predicción de progresión de la enfermedad
- Herramientas de búsqueda de pacientes
- Herramientas de modelización de respuesta al tratamiento
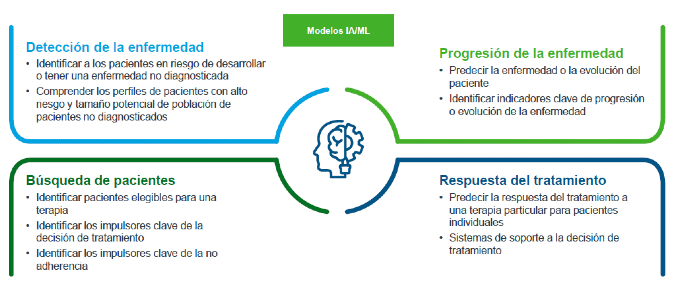
En esta sección compartiremos un caso práctico de cada una de estas áreas para poder reflejar el alto potencial que tiene la IA/ML.
1. Detección de una enfermedad: un ejemplo de uso de la IA/ML en el ámbito de la detección de una enfermedad lo podemos encontrar en el cáncer de mama. Éste es un tipo de cáncer que afecta a las células de las mamas y es uno de los tipos de cáncer más frecuente. El cáncer de mama se puede diseminar en ocasiones a los ganglios linfáticos (metástasis). Es por ello que se suelen analizar los ganglios centinela ya que son los primeros ganglios linfáticos hacia los que se disemina el tumor. Con este procedimiento se puede determinar el grado de disección axilar que se requiere realizar para extirpar los ganglios linfáticos afectados.
En este caso, el objetivo era poder detectar tejidos metastásicos en los ganglios linfáticos en base a los hallazgos de exploraciones histopatológicas de manera precisa. Para el diseño de la solución se usaron 327.680 imágenes en color extraídas de exploraciones histopatológicas de secciones de ganglios linfáticos con un marcador binario que indicaba la presencia o ausencia de tejido metastásico. Estas imágenes se combinaron con la aplicación y optimización de modelos de redes neuronales convolucionales de aprendizaje profundo de última generación como ResNet, DenseNet, MobileNet y Exception.
El uso de las técnicas de IA/ML permitió poder detectar los tejidos metastásicos con una precisión muy alta (97.8%). Las nuevas metodologías también permitieron entender qué partes de una imagen se utilizan para identificar tejidos metastásicos, con el fin de validar las predicciones del modelo.
Estudios de este tipo demuestran la relevancia de incorporar la IA/ML en el diseño de sistemas de apoyo para la toma de decisiones de los profesionales de la salud.
2. Progresión de la enfermedad: otra de las posibles aplicaciones de la IA/ML es poder determinar la progresión de la enfermedad. En este caso, el objetivo era poder determinar la progresión de la pandemia de la COVID-19 que nos lleva afectando desde inicios del 2020. Concretamente, el objetivo era estimar el impacto que tiene la vacunación de la COVID-19 en hospitalizaciones y uso de UCIs en España a causa de esta enfermedad.
Para estimar dicho impacto se combinaron modelos epidemiológicos y técnicas de IA/ML que predecían, en primer lugar, las muertes asociadas a la COVID-19 y, en segundo lugar, las hospitalizaciones e ingresos en UCI a nivel nacional teniendo en cuenta la variabilidad en la dinámica de la enfermedad en los diferentes grupos de edad (el nivel de hospitalizaciones y uso de UCIs es mayor en los grupos de más avanzada edad) y la estrategia de vacunación seguida por parte del gobierno (en este caso, empezando por los grupos de mayor edad y priorizado las doble vacunación). En este análisis se consideraron 4 escenarios diferentes en función de la velocidad de despliegue del plan de vacunación y la predisposición por parte de la población general en España a recibir la vacuna.
El modelo desarrollado permitió predecir la evolución de las hospitalizaciones y el uso de UCIs por grupo de edad y en función de los diferentes escenarios considerados con un alto nivel de precisión. Los valores del R2 para los modelos de predicción de hospitalizaciones e ingresos en UCI eran de 0,82 y 0,88 respectivamente.
Este tipo de modelizaciones en las que se combinan modelos epidemiológicos y modelos de IA/ML con impacto en resultados sanitarios pueden ser de gran utilidad para generar y explotar la evidencia en vida real.
3. Identificación de pacientes: a menudo nos encontramos con dificultades para identificar los pacientes candidatos a un tratamiento (p.e. complejidad en el diagnóstico, diferentes rutas asistenciales para llegar al diagnóstico/tratamiento, etc.). Este es otro de los aspectos en los que la IA/ML puede ser clave.
En este ejemplo, el objetivo marcado era, por una parte, poder identificar grupos de pacientes que se podían beneficiar de un tratamiento en concreto y, por otra parte, ser capaces de identificar patrones en la progresión de la enfermedad que desembocan en la indicación concreta para la cual los pacientes podían beneficiarse de dicho tratamiento. Asimismo, también era relevante entender las dinámicas de tratamiento para la patología y de los pacientes que no recibían ningún tipo de tratamiento y de los que estaban tratados con otras alternativas menos eficaces dadas sus características.
Para dar respuesta a esta necesidad, se combinó información anonimizada a nivel paciente junto a técnicas de IA/ML. De esta manera se desarrolló un modelo que permitía identificar aquellos pacientes candidatos a la terapia, sus características y los patrones que hacen que un paciente evolucione y acabe siendo un potencial candidato a beneficiarse del tratamiento.
4. Respuesta al tratamiento: en un futuro próximo, cada vez será más relevante demostrar el valor de un tratamiento en su uso en vida real para diferenciarse del resto de opciones terapéuticas disponibles para una patología en concreto. En este caso, el objetivo era evaluar la superioridad en seguridad y eficacia de un fármaco indicado en pacientes con fibrilación auricular para prevenir los accidentes cerebrovasculares, frente a otros fármacos con la misma indicación, y entender qué grupos de pacientes se podrían beneficiar más de un tratamiento u otro.
La fibrilación auricular es la arritmia cardíaca más frecuente y una de las principales causas de los accidentes cerebrovasculares isquémicos. La prevalencia de la fibrilación auricular mundial estimada en 2017 era de 37,6 millones a nivel mundial y el coste directo e indirecto asociado a esta patología está en constante crecimiento.
Para acometer los objetivos de este ejemplo se combinó información anonimizada a nivel paciente con un histórico mínimo de un año con técnicas de IA/ML. Se desarrollaron dos modelos predictivos diferentes:
• El primer modelo predecía el riesgo de ictus y de hemorragia intracraneal en función del tratamiento que el paciente estuviese recibiendo y las características de dicho paciente. Este modelo permitía demostrar la mayor eficacia y seguridad de un tratamiento versus el resto.
• El segundo modelo tenía como objetivo identificar aquellos pacientes que, por sus características, se podrían beneficiar de un tratamiento en concreto. Como ya se ha comentado con anterioridad, la incorporación de técnicas de IA/ML en los sistemas de soporte a la toma de decisiones para los profesionales de la salud son clave.
Conclusiones
El desarrollo de RWE va a ser un componente estratégico para cualquier nuevo lanzamiento. En este sentido, el desarrollo de modelos de IA/ML permite la generación de un tipo de “pruebas” que hasta ahora no podíamos trabajar, ya sea porque no se podía estructurar la información de partida o porque no existían herramientas de cálculo que pudieran analizar los datos y crear los modelos predictivos/prescriptivos.
La estrategia de desarrollo de evidencia clínica cada vez va a tener que ir más de la mano de la estrategia comercial.
Consecuentemente, es clave para cualquier product manager estar al día de los últimos avances en el campo de la generación de evidencia con el objetivo de poder desarrollar una estrategia holística de producto y con el paciente como el centro de esta estrategia.
















