El Gobierno autoriza la venta al público sin receta de test de antígenos en farmacias
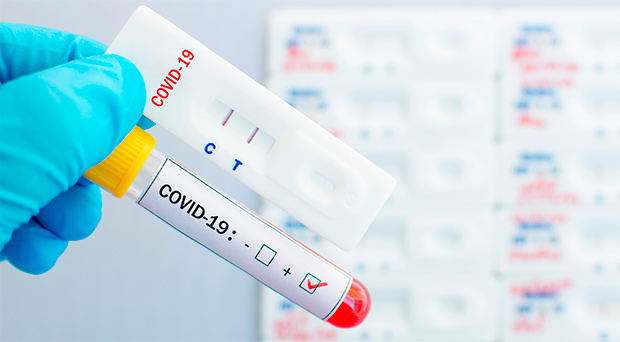
El Consejo de Ministros, ha aprobado este martes el Real Decreto por el que se modifica el RD 1662/2000, del 29 de septiembre, sobre productos sanitarios para diagnóstico in vitro, con objeto de regular la venta al público y la publicidad de los productos de autodiagnóstico de la COVID-19. A partir de su publicación en el Boletín Oficial del Estado, se podrán adquirir libremente tanto los test de anticuerpos como los test de antígenos avalados por la Agencia Española del Medicamento (AEMPS) para la venta exclusiva en farmacias.
En rueda de prensa, la portavoz del Gobierno y ministra de Política Territorial, Isabel Rodríguez, ha calificado esta decisión como "una medida muy reclamada y deseada", y ha felicitado al Ministerio de Sanidad por el acuerdo alcanzado con los colegios de farmacéuticos y la industria farmacéutica.
Rodríguez ha resaltado que con su venta sin receta se permite a los ciudadanos hacer, "a título personal, un ejercicio de prevención" ante posibles contagios. En cualquier caso, ha insistido en que si el test da positivo deberá ser notificado al centro de salud para "chequear de nuevo" el diagnóstico y poder registrarlo ante el sistema sanitario.
La ministra de Sanidad, Carolina Darias, reivindicó la semana pasada que "se hace necesario aumentar la capacidad diagnóstica para identificar de forma más rápida sospecha de casos positivos e incluso de asintomáticos, como está ocurriendo en la población de 12 a 29 años, y controlar de la manera más eficaz posible la progresión de la pandemia".
"La exigencia de prescripción constituía una barrera", admitió la ministra. Este Real Decreto-Ley recibió el pasado viernes 8 de julio el preceptivo dictamen positivo del Consejo de Estado.
Darias justificó por qué en España han tardado tanto tiempo en llegar estas pruebas diagnósticas, en contraste con otros países europeos como Francia o Alemania, donde se pueden adquirir en farmacias, sin prescripción y a módicos precios, desde hace meses.
"Hasta que no teníamos la existencia de test de autodiagnóstico con marcado CE no podíamos autorizarlo. Estábamos esperando la llegada al mercado. Tan pronto llegaron nos pusimos en marcha con la tramitación del Real Decreto-Ley, que tiene su proceso. También estábamos esperando al dictamen del Consejo de Estado", explicó.
Según las cifras aportadas por la ministra, habrá disponibles hasta cinco test con marcados CE y otros 11 con marcado en Europa, mientras que otros 39 están en investigación.
Las pruebas de autodiagnóstico de la COVID-19 se unirán a otros test que tampoco necesitan receta, como los del embarazo y de la fertilidad, así como los destinados a la determinación de la glucemia o la detección del VIH. Al igual que estos productos, los test para detectar la COVID-19 tendrán permitido realizar publicidad.










 &
& 
