Disponible en España Tecentriq, primera inmunoterapia antiPD-L1 para tumores de pulmón y vejiga en estadio metastásico
Podrán beneficiarse de Tecentriq los pacientes con cáncer de pulmón no microcítico (CPNM), localmente avanzado o metastásico que hayan recibido un tratamiento previo.
Son también candidatos al tratamiento los pacientes con carcinoma urotelial metastásico tratados previamente con quimioterapia basada en platino.
Hasta su aprobación, no había ninguna inmunoterapia disponible para tratar el cáncer de vejiga avanzado.
La inmunoterapia frente al cáncer representa un área de investigación en constante expansión, que está cambiando la forma en que se aborda actualmente el tratamiento de cada vez más tumores. Hace escasos días, el Ministerio de Sanidad, Servicios Sociales e Igualdad pone a disposición de los pacientes un nuevo tipo de inmunoterapia para tumores de pulmón y vejiga en estado metastásico: un inhibidor de PD-L1. Este anticuerpo monoclonal antiPD-L1 constituye un nuevo avance dentro del esfuerzo investigador que desde hace una década va aportando evidencias de los beneficios de activar el sistema inmune frente a las células tumorales. El primero de la familia de inhibidores de PD-L1 en llegar ha sido atezolizumab (Tecentriq), con una doble indicación para tumores de pulmón y vejiga en estados avanzados o metastásicos. Se trata de la primera inmunoterapia para este tumor urológico y el primer antiPD-L1 para el carcinoma pulmonar.
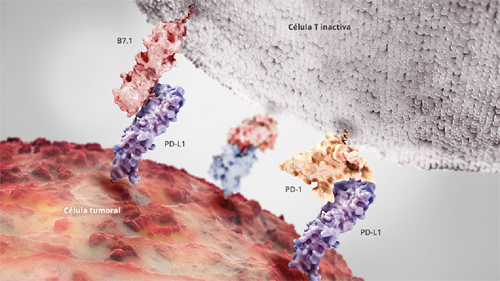
Tecentriq se ha diseñado para unirse a una proteína denominada PD-L1 presente en la superficie de las células tumorales, bloqueando su interacción con los receptores PD-1 y B7.1. De ese modo, hace posible que las células del sistema inmune detecten y destruyan las células tumorales.
La doctora Annarita Gabriele, directora médico de Roche España, subraya que el desarrollo de una inmunoterapia pionera en su mecanismo de acción como es atezolizumab es un ejemplo más del compromiso de Roche, desde hace varias décadas, por mantenerse en la vanguardia de la investigación oncológica. “Actualmente”, explica, “dedicamos grandes esfuerzos a la I+D de opciones terapéuticas innovadoras que ayuden al sistema inmune del propio paciente a combatir el cáncer. Para ello aportamos más de 7.000 millones de euros al año de la inversión total en I+D a la inmunoterapia oncológica. Nuestro programa de investigación cuenta con más de 20 moléculas candidatas, 12 de las cuales están siendo evaluadas en ensayos clínicos y se dirigen a los tres perfiles tumorales. En total son más 60 ensayos en marcha, tanto en monoterapia como en combinación”.
Gabriele añade que la participación de los hospitales españoles ha sido esencial en la investigación clínica de la molécula para ambas indicaciones. “España figura entre los tres países con más peso en este sentido, con un total de 34 centros de todo el territorio nacional en los cuatro estudios que han avalado las autorizaciones del fármaco tanto en pulmón, con los ensayos clínicos OAK y POPLAR, como en vejiga con IMvigor210 e IMvigor211”.
Primer antiPD-L1 en cáncer de pulmón
La indicación financiada por el Ministerio para Tecentriq es en monoterapia para el cáncer de pulmón no microcítico (CPNM) localmente avanzado o metastásico en pacientes tratados previamente con quimioterapia, independientemente del nivel de expresión de PD-L1. Es preciso que los pacientes con la mutación EGFR o ALK positiva hayan recibido una terapia dirigida antes de ser tratados con esta nueva terapia. La aprobación se ha basado en los resultados de los estudios aleatorizados fase III OAK y fase II POPLAR. Los resultados del OAK demostraron que los pacientes tratados con Tecentriq® alcanzaban de una mediana de supervivencia de 13.8 meses, logrando 4.2 meses más que la que consiguen los que recibieron la quimioterapia docetaxel (mediana de supervivencia global (SG): 13.8 vs 9.6 meses; hazard ratio [HR] = 0.73, intervalo de confianza [IC] al 95%: 0.62, 0.87).
En palabras del doctor Mariano Provencio, presidente del Grupo Español de Cáncer de Pulmón (GECP) y jefe del Servicio de Oncología del Hospital Puerta de Hierro de Madrid, “la llegada de la primera molécula antiPD-L1 en monoterapia va a suponer que muchos pacientes con cáncer de pulmón no microcítico en segunda línea puedan beneficiarse de este tratamiento. Se trata de un avance muy representativo en el mundo de la Oncología, ya que, aparte de una mayor eficacia en términos de supervivencia global, estamos ante una estrategia más segura que provoca menos efectos secundarios que la quimioterapia”.
Según este experto, la irrupción de la inmunoterapia ya puede calificarse de nuevo hito de la Oncología moderna y, de forma específica, en el abordaje del cáncer de pulmón donde, subraya, “hoy podemos empezar a hablar de largos supervivientes en pacientes tratados con este tipo de fármacos, obteniéndose en algunos casos tasas de supervivencia antes nunca vistas”.
Primera inmunoterapia disponible para el cáncer de vejiga avanzado
La disponibilidad de la primera inmunoterapia en cáncer de vejiga avanzado supone poder incorporar una nueva opción al arsenal terapéutico de un tumor de mal pronóstico que apenas ha registrado avances de relevancia en los últimos 30 años. La indicación aprobada por el Ministerio para Tecentriq® es en monoterapia para adultos con carcinoma urotelial localmente avanzado o metastásico (CUm) que han sido tratados previamente con quimioterapia basada en platino, independientemente del nivel de expresión de PD-L1. La autorización se ha basado en los resultados del estudio aleatorizado fase III IMvigor211 y de la cohorte 2 del estudio de un solo brazo fase II IMvigor210.
Aunque el estudio IMvigor211 no alcanzó su objetivo principal de supervivencia global en comparación con quimioterapia, mostró que la mediana de la duración de la respuesta, uno de los objetivos secundarios del ensayo, fue de 21,7 meses (IC 95%: 13.0, 21.7) en los pacientes tratados con Tecentriq en comparación con 7.4 meses (IC 95%: 6.1, 10.3) del grupo de quimioterapia. La mayoría de los pacientes que respondieron al tratamiento con Tecentriq (63%) continuaron respondiendo al mismo, en comparación con el 21% de los tratados con quimioterapia.
El doctor José Ángel Arranz, presidente del Grupo Español de Oncología Genitourinaria (SOGUG) y jefe de Sección del Servicio de Oncología Médica del Hospital Gregorio Marañón de Madrid, considera que la disponibilidad de fármacos como Tecentriq supone “un avance muy importante para un tumor como el carcinoma de vejiga metastásico que de manera tradicional se ha tratado con quimioterapia tanto en primera línea como en los casos de progresión tras un tratamiento sistémico previo. Una de las causas de dicha progresión consiste en que el tumor es capaz de desarrollar mecanismos de ocultación y escape de las células del sistema inmunológico encargadas de su identificación y destrucción. Ahora, con este tipo de inmunoterapias, somos capaces de reclutar de nuevo a estas células defensivas del sistema inmune para que ayuden en la lucha contra el cáncer”.
La verdadera magnitud del beneficio clínico que puede llegar a aportar los antiPD-L1 requiere aún tiempo, dado que la mayoría de estudios aún están en marcha, según explica el doctor Arranz. “Estamos comprobando que los pacientes que progresan tras un tratamiento previo y reciben inmunoterapia tienen mejor tasa de respuesta que si reciben quimioterapia. A esto hay que sumar que, por lo general, estos nuevos fármacos son mejor tolerados que la quimioterapia clásica, una ventaja de especial importancia para pacientes que puedan estar debilitados porque presentan otros problemas de salud asociados. En algunos casos, además de mayor respuesta, se consigue un incremento de la supervivencia”, añade el doctor Arranz que como presidente de SOGUG recuerda asimismo que la amplia participación de hospitales españoles en el desarrollo clínico de Tecentriq y otras inmunoterapias ha hecho posible que la mayoría de pacientes del país haya tenido acceso precoz a estas innovaciones.










 &
& 
